Wie entwickelt sich ein dysplastisches Hüftgelenk?
Die Entwicklung der Hüftgelenke wird massgeblich durch zwei Komponenten beeinflusst:
- durch die Erbanlage und
- durch die Ernährung des Hundes.
Zur Erbanlage: Erwiesen ist, dass sich HD häufig in Form einer übermässigen Lockerheit oder Instabilität des Hüftgelenkes zeigt, welche die Entwicklung von Arthrose begünstigt. So wie wir beim Tragen von zu grossen Schuhen bald Blasen oder einen tüchtigen Muskelkater einfangen, nimmt auch das Hüftgelenk Schaden, wenn der Oberschenkelkopf dauernd in der Gelenkspfanne herum rutscht. Technisch ausgedrückt, erfährt ein lockeres Hüftgelenk dieselben Veränderungen wie ein lockeres Radlager: Es wird ausgeschlagen. Beim jungen Hund zeigen sich deshalb die stärksten Veränderungen an der Gelenkspfanne: sie weitet sich auf und flacht sich ab. Damit wird der Oberschenkelkopf nicht mehr korrekt geführt, es entwickelt sich eine Arthrose. Ein straffes Gelenk entwickelt keine HD.
Zur Ernährung: Eine Fütterung, welche den Hund sehr schnell wachsen und insbesondere schnell an Gewicht zunehmen lässt, fördert die fehlerhafte Entwicklung der Gelenke nachweislich, wenn der Hund auf Grund seiner genetischen Anlage zu HD neigt. Ein Hund mit einer Veranlagung zu HD kann sich also die Hüftgelenksarthrose geradezu anfressen! Diese Erkenntnis ist theoretisch für einen Züchter von grossem Nutzen. Durch Überfütterung seiner Hunde könnte er jene entdecken, die trotz übermässiger Gewichtszunahme gute Gelenke entwickeln, also genetisch unterdurchschnittlich stark mit HD-Genen belastet sind. Denn ein genetisch HD-gesunder Hund wird auch durch unsachgemässe Fütterung kaum je HD entwickeln.
Umgekehrt ist es bei einem Hund mit Veranlagung zu HD möglich, durch eine kalorienmässig zurückhaltende und ausgewogene Fütterung das Ausmass der Krankheit zu mildern. Es ist erwiesen, dass Hunde, die langsam wachsen, weniger schwer an HD erkranken als ihre schneller wachsenden und damit schwereren Wurfgeschwister. Besonders wichtig ist dabei, im Futter ein Überangebot von Kalzium (Futterkalk) zu vermeiden. Heutige Fertigfutter enthalten genügend Kalzium, so dass kein Futterkalk zugefüttert werden sollte. Hazewinkel erachtet 0.8% Kalzium auf Trockengewichtsbasis (0.76 g Kalzium pro 400 kcal. bzw. 1700 kJ.) als ausreichend. Das Kalzium/Phosphor-Verhältnis sollte etwa 1:1 betragen (zit. Wess). Optimierte Fütterung hilft zwar, dass ein einzelner Hund trotz ungünstigen Erbanlagen eine grössere Chance hat, akzeptable Hüftgelenke zu entwickeln und ein weit¬gehend normales und schmerzfreies Leben zu führen. Für zukünftige Zuchttiere ist diese Taktik aber nicht geeignet, da die genetische Belastung für HD damit nicht aufgedeckt werden kann. Kommen derart aufgezogene, erblich aber belastete Hunde zum Zuchteinsatz, wird die Veranlagung zu HD an die nächste Generation weitergegeben. Die Folge ist, dass unter den Nachkommen von Hunden mit guten Hüftgelenken dysplastische Nachkommen auftreten.
In Züchterkreisen wird vermutet, dass die jugendliche Aktivität der Welpen HD verursachen könne. Bis heute konnte diese Theorie nicht bewiesen werden. Ein gesundes Hüftgelenk wird durch die normale Bewegung und durch Spielen mit Artgenossen nicht geschädigt. Sicher ist es vernünftig, eine massive Überbeanspruchung des noch unreifen Skeletts des Junghundes zu vermeiden, da ein Knochen im Wachstum weniger belastbar ist, als das Skelett eines ausgewachsenen Tieres.
Die Diagnose HD lässt sich anhand von Röntgenaufnahmen des Hüftgelenks stellen. Sichtbare Veränderungen können an der Gelenkspfanne, am Oberschenkelkopf oder an beiden Knochen auftreten. Bei jungen Hunden ist gelegentlich nur ein auffällig lockeres Hüftgelenk zu beobachten, bei dem der Oberschenkelkopf nicht korrekt in der Gelenkspfanne liegt.
Aufgrund der Veränderungen auf dem Röntgenbild werden fünf Schweregrade von HD unterschieden.
| HD-Grad (FCI) |
|---|
| A = HD-frei |
| B = Übergangsform |
| C = leichtgradige HD |
| D = mittelgradige HD |
| E = hochgradige HD |
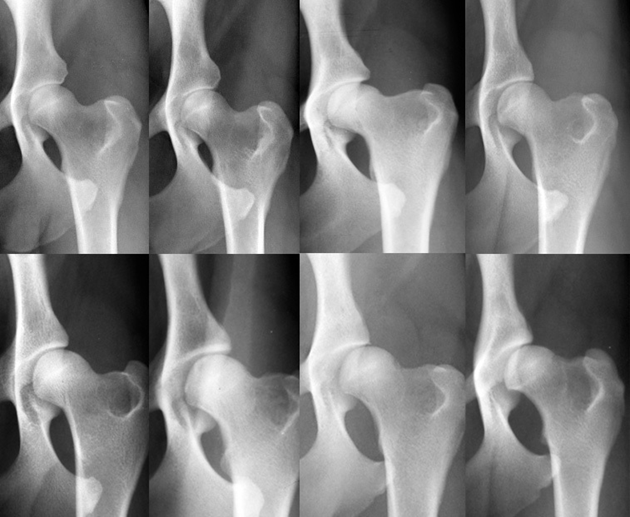
Abb. 1: Verschiedene Hüftgelenke, von A, normal bis E, hochgradig dysplastisch (Bildfolge Dr. A. Vezzoni, mit bestem Dank).
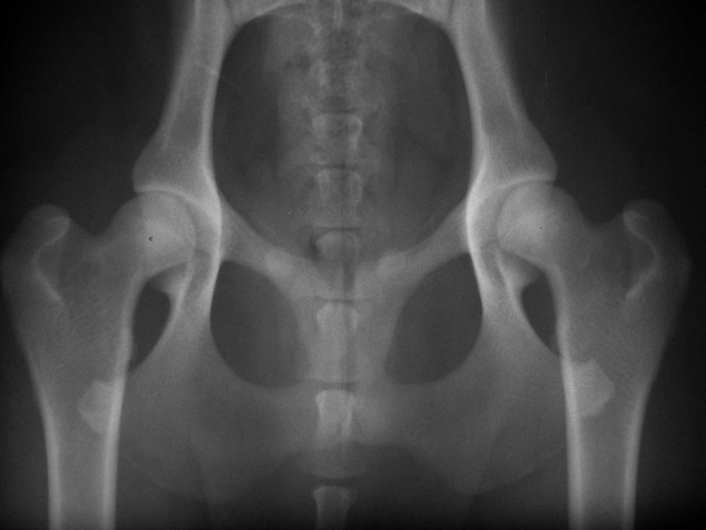
Abb. 2: Exzellente Hüftgelenke (Grad A) bei einem 15 Monate alten Labrador Retriever der Blindenführhundeschule Allschwil. Bei beiden Hüftgelenken sitzt der runde Oberschenkelkopf tief in der Pfanne. Der Vorderrand der Pfanne (oben) liegt dem Kopf exakt an, der Gelenkspalt ist schmal, der vordere Pfannenknochen gleichmässig schmal. Durch umfassende Nachzuchtkontrolle mit rigider Auslese der Zuchttiere aufgrund der Qualität der Nachkommen weisen weit über 90% der Hunde der Schule hervorragende Hüftgelenke (und Ellbogengelenke) auf.
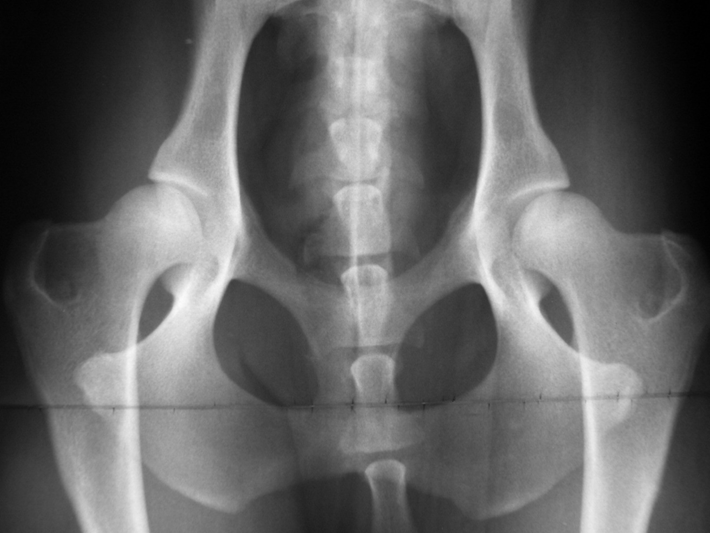
Abb. 3: Englischer Setter mit HD Grad C. Der Oberschenkelkopf ist zwar rund, rutscht aber etwas aus der Pfanne. Der vordere Pfannenrand läuft horizontal aus. Solche Hunde neigen im Laufe des Lebens zu Hüfgelenksarthrose.
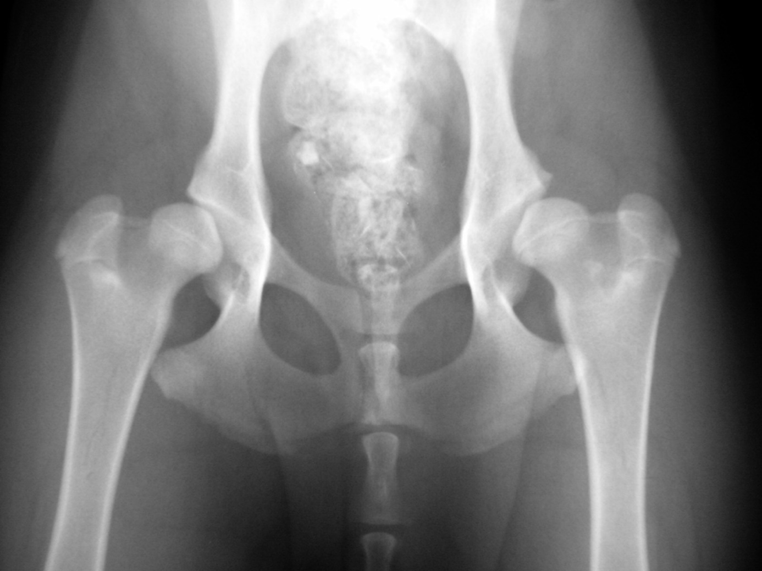
Abb. 4: 8 Monate alter Mischlingshund mit hochgradiger HD (Grad E). Der Kopf ist kantig, oben abgeflacht und weitgehend aus der Pfanne herausgerutscht, die Pfanne selber oben stark abgeflacht, sogar fliehend. Am Vorderrand der linken Pfanne (im Bild rechts) hat sich eine Randzacke ausgebildet, ein untrügliches Zeichen von schwerer Arthrose.
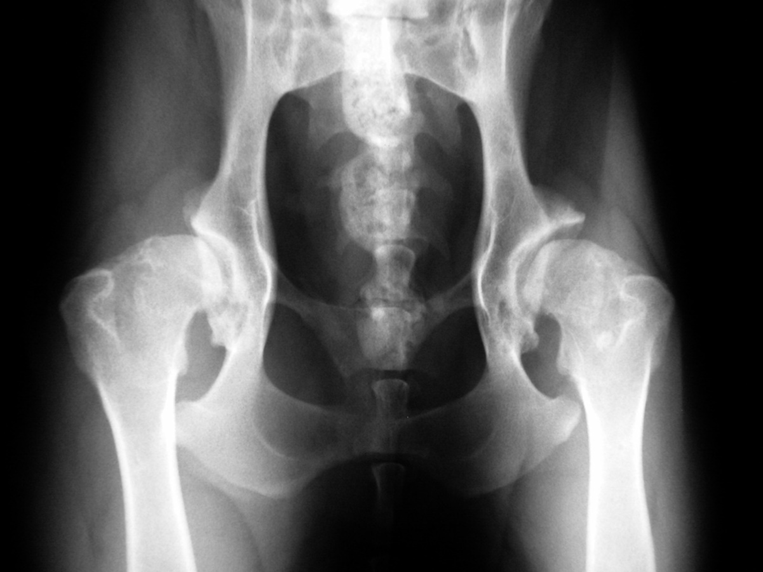
Abb. 5: Derselbe Hund im Alter von 5 Jahren. Die Oberschenkelköpfe sind nun hochgradig verformt und berühren die Pfannen nur noch knapp. Die Oberschenkelhälse sind massiv verdickt und verformt, die Morganlinien sind als breite Knochenleiste erkennbar. Beide Pfannen sind stark abgeflacht und haben insbesondere rechts hochgradige arthrotische Zubildungen entwickelt.
Wie häufig kommt HD bei den untersuchten Hunden vor?
Zwischen 1991 und 1994 wurden von den beiden HD-Kommissionen 3749 Hunde untersucht. Die HD-Resultate sind in Abbildung 6 dargestellt. HD trat bei Rüden und Hündinnen gleich häufig auf, das Auftreten hängt also nicht vom Geschlecht des Tieres ab. Ein Viertel der untersuchten Hunde wurde als HD-frei, und ein Drittel als Übergangsform beurteilt. Damit gehörten beinahe 60% der Hunde zu den beiden Graden, die mit gutem Gewissen zur Zucht verwendet werden können. Mehr als ein Viertel der Hunde wurde als leicht dysplastisch (HD-Grad C) bewertet, sie sollten nicht oder nur in begründeten Fällen zur Zucht verwendet werden. Rund jeder 7. Hund fiel sogar in die HD-Grade D und E mit ausgeprägten Gelenksveränderungen. Derartige Tiere sind von der Zucht ausgeschlossen.
Die neueren Daten von der HD-Kommission Zürich aus den Jahren 1995 bis 2000 zeigen einen deutlichen Rückgang der HD-Häufigkeit und auch des Schweregrades (Abbildung 6). Rund 70% der Hunde können zur Zucht empfohlen werden. Nur noch jeder 11. Hund leidet an einer mittel- oder hochgradigen HD, was aber immer noch zu viel ist. Die langjährigen Bemühungen der Hundebesitzer und Züchter beginnen trotzdem Früchte zu tragen!
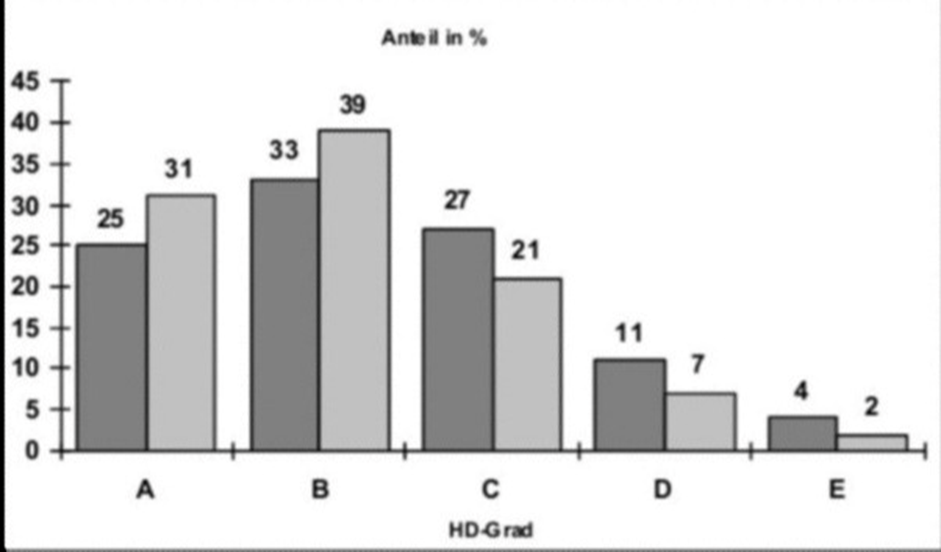
Abb. 6: HD-Verteilung von 3749 Hunden der Jahre 1991-1994 (dunkel) und von 7394 Hunden der Jahre 1995-2000 (hell) in %
Kommt HD bei allen Rassen gleich häufig vor?
Der Anteil dysplastischer Hunde ist bei den verschiedenen Rassen sehr unterschiedlich, die Verteilung ist in Abbildung 7 dargestellt. Die besten Hüftgelenke wies der Siberian Husky auf, gefolgt von den Collies und den Belgischen Schäferhunden. Dysplasiefrei waren rund zwei Drittel aller Hovawarte, Flat Coated Retriever, Leonberger und Rottweiler, über die Hälfte der Labrador Retriever und Berner Sennenhunde, die Hälfte der Golden Retriever, Neufundländer und der Deutschen Schäferhunde, aber weniger als die Hälfte der untersuchten Boxer. Bei Bernhardinern, sowie English und Gordon Settern lag die HD-Rate bei erschreckend hohen 60-70%. Durch die intensiven Bemühungen der Züchter in den vergangenen Jahren ist die Zahl dysplastischer Hunde insbesondere bei den Bernhardinern aber stark zurückgegangen.
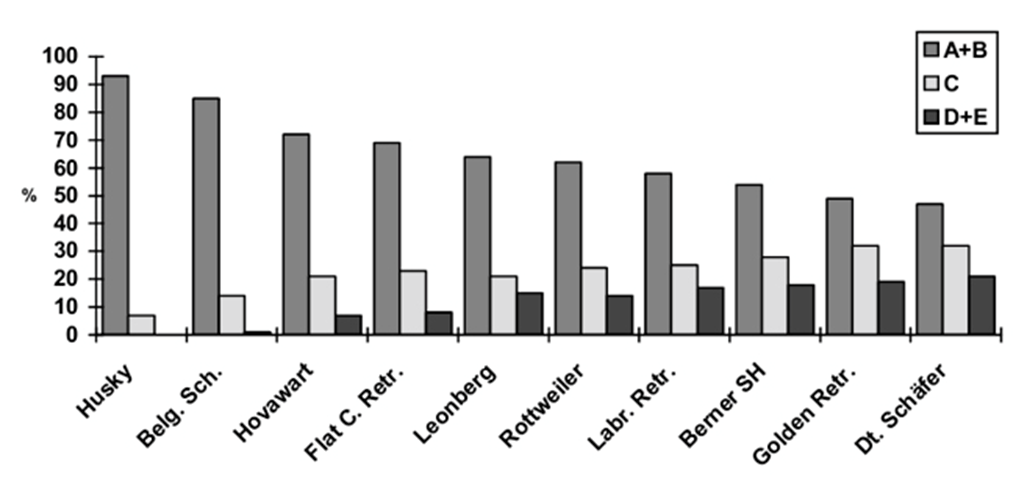
Abb. 7: HD-Verteilung in % in den 10 häufigsten Rassen (1991-1994)
Wieso bestehen derartige Rassenunterschiede in der HD-Häufigkeit?
Bei verschiedenen Rassen kam die Krankheit schon zu Beginn der HD-Bekämpfung selten vor. Besonders Schlittenhunde oder Jagdhunde, die seit jeher auf eine lebenslange Leistungsfähigkeit gezüchtet worden sind, zeigen kaum HD; Hunde, die nach anstrengender Arbeit lahmten, wurden gar nicht erst zur Zucht verwendet. Beim Hovawart waren schon vor der Einführung der HD-Kontrolle viele Hunde dysplasiefrei, deshalb konnte seit jeher eine strenge Selektion durchgeführt werden.
Die wichtigsten Gründe für den hohen HD-Anteil in verschiedenen Rassen sind die Verwendung dysplastischer Elterntiere (HD Grad C) zur Zucht und das weitgehende Fehlen einer Nachzuchtkontrolle. Beim Bernhardiner rächte es sich, dass die Zuchttiere jahrelang nicht auf HD untersucht und Hunde trotz ausgeprägter HD zur Zucht verwendet worden sind. Bei vielen Rassen wurde bei der Auswahl von Zuchthunden zudem lange Zeit zu stark dem Exterieur und dem Kampftrieb Bedeutung zugemessen. Gesundheitliche Aspekte wurden kaum berücksichtigt. Durch die intensive Aufklärungsarbeit hat sich diese Sichtweise aber wesentlich geändert, heute wird der Gesundheit der Tiere mehr Beachtung geschenkt.
Der Anteil dysplastischer Hunde ist vermutlich höher als es die Zahlen in Abbildung 6 widerspiegeln. Röntgenbilder von schwer dysplastischen Hunden werden nur selten zur offiziellen Beurteilung eingesandt, da die Züchter um ihren guten Ruf als HD-freie Zuchtstätte fürchten. Auch Bilder von dysplastischen Tieren, die vor der Körung wegen Bewegungsstörungen geröntgt werden, gelangen kaum je zur Auswertung. Dieses Vorgehen behindert den Fortschritt enorm, da es dadurch nicht möglich ist, die Zuchterfolge zu überprüfen und die Zuchtvorschriften anzupassen. Zudem werden Berechnungen zur Erblichkeit (Heritabilität) der HD verfälscht. Die Züchter und Hundebesitzer betrügen sich so selber um ihre Bemühungen, die HD-Häufigkeit nachhaltig zu senken.
Wieso kommt die HD immer noch häufig vor?
Wenn eine Krankheit in einer Rasse bekämpft werden soll, dürfen Träger der Krankheit nicht zur Zucht verwendet werden. Der Einsatz von dysplastischen Tieren zur Zucht ist somit unverantwortlich. Sie widerspricht dem Gedanken des Tierschutzes, der besagt, nur Tiere zu züchten, die frei sind von Krankheiten, welche die Lebensqualität einschränken. Dazu gehört auch die schmerzhafte HD. Jeder Käufer eines rassereinen Hundes hat grundsätzlich Anrecht auf einen gesunden und damit dysplasiefreien Hund. Solange jedoch C-Hunde als zuchttauglich erklärt werden, lässt sich die HD-Häufigkeit bei den Nachkommen nicht weiter senken. Erschwerend kommt dazu, dass der Zuchtwert eines Tieres für das Merkmal HD nicht nur allein von der Qualität seiner eigenen Hüftgelenke abhängt, sondern auch von derjenigen seiner nahen Verwandten wie der Eltern und der Geschwister. Nur wenn ihre HD-Ergebnisse auch berücksichtigt werden, lässt die Hüftgelenksqualität der Nachkommen schätzungsweise voraussagen.
Wie kann HD verhindert werden?
Bei einem einzelnen Hund kann jeder Züchter und Hundebesitzer durch eine sorgfältige Fütterung des jungen Hundes direkten Einfluss auf die Entwicklung der Hüftgelenke nehmen. Es ist nachgewiesen, dass eine zu schnelle Gewichtszunahme in den ersten 10 Lebensmonaten die Fehlentwicklung der Gelenke fördert. Zu grosse Mengen von Kalzium im Futter begünstigen die Ausbildung der HD nachweislich. Vermutlich sind auch zu grosse Futterrationen nachteilig. Wird ein HD-gefährdeter Hund im Wachstum noch übermässig beansprucht, kann sich die HD weiter verschlimmern. Hingegen scheinen weder die endgültige Körpergrösse noch das endgültige Körpergewicht des Hundes einen wesentlichen Einfluss auf die Hüftgelenke zu haben. Starkes Übergewicht bei einem dysplastischen Hund verschlimmert aber die Schmerzen noch.
Unter den Hundebesitzern machen viele „Geheimrezepte“ die Runde, die eine Heilung versprechen. Leider entpuppen sich diese Versprechen fast immer als wirkungslos. So kann z.B. Vitamin C eine HD nicht verhindern. Auch die allermeisten gängigen Futtermittelzusätze haben keine nachweisbaren Wirkungen auf ein dysplastisches Gelenk. Zufütterung von Glukosaminsulfat kann bei gewissen Hunden die Schmerzen lindern, die Arthrose kann aber nicht geheilt werden. Die Substanz wirkt nicht bei allen Hunden und auch nicht bei allen gleich gut. Nebenwirkungen sind keine bekannt. Chondroitinsulfat wirkt weniger gut, da es nicht unverändert durch die Darmwand aufgenommen werden kann. Goldimplantate um die Hüftgelenke sind nach neusten Erkenntnissen ebenfalls unwirksam. Im besten Fall kann Gold die Entzündung, nicht aber die bestehenden Veränderungen lindern. Grössere seriöse Doppelblindstudien sind bis heute aber nicht durchgeführt worden.
Die langfristig wirksamste Massnahme zur Verringerung der HD ist die Einführung und Durchsetzung von Paarungsbeschränkungen. Der Anteil gesunder Nachkommen steigt an, wenn nicht nur der HD-Grad des Tieres selber (die sogenannte Eigenleistung), sondern auch die HD-Resultate seiner Geschwister und insbesondere seiner bereits geborenen Nachkommen mit berücksichtigt werden. Mit Hilfe einer derartigen Zuchtwertschätzung könnte der Züchter für sein Zuchttier einen geeigneten Partner auswählen, ohne seinen Hund wegen HD-Belastung von vorne herein aus der Zucht nehmen zu müssen. Dieses Konzept wird als strategische Paarung bezeichnet und hat zum Ziel, nur noch Welpen zu züchten, die ein unterdurchschnittliches Risiko haben, an HD zu erkranken. Die Zuchtzulassung wird damit nicht mehr vom HD-Resultat des Einzeltieres abhängig gemacht, sondern vom HD-Risiko für die Nachkommen einer Paarung. Diese Methode der Zuchtselektion hat sich in der Nutztierzucht als äusserst erfolgreich erwiesen. Sie wurde in den vergangenen Jahren von vielen Hunderasseklubs eingeführt. In Deutschland haben bereits über 50 Rassehundeklubs diesen Weg beschritten. Der Erfolg hängt von der zu bekämpfender Krankheit ab. Die strategische Paarung ist nur erfolgreich, wenn zuvor eine klare Zuchtstrategie erarbeitet und die Paarungsbeschränkungen konsequent eingehalten werden.
In neuester Zeit sind Ansätze zur molekulargenetischen Aufklärung der HD ins Zentrum des Interesses gerückt. Erfasst und analysiert werden unzählige Genmarker (sogenannte Mikrosatelliten) mit Hilfe des sogenannten Single Nucleotide Polymorphismus (SNPs). Vorläufige Ergebnisse zeigen, dass die Entwicklung des Hüftgelenks beim Hund von vielen Genen beeinflusst wird, die auf verschiedenen Chromosomen lokalisiert sind. Gewisse Gene scheinen einen deutlich grösseren Einfluss auf die Gelenksentwicklung zu haben als andere. Sie werden als Dominanzgene bezeichnet. Ziel dieser Studien ist es, den Entscheid, ob ein Tier zur Zucht verwendet werden kann, nicht mehr allein auf den Röntgenbefund des erwachsenen Tieres, sondern auch auf seine genetischen Eigenschaften abzustützen, also seine genomischen Zuchtwert zu bestimmen. Da die Gene schon bei der Geburt unveränderlich vorliegen, könnten Welpen jeden Alters darauf hin untersucht werden. Der Züchter müsste also nicht mehr den Röntgenbefund abwarten, um zu erfahren, welche seiner Tiere später wahrscheinlich zur Zucht (zumindest was die HD betrifft) geeignet sein werden. Wenn die Prognosen zutreffen, sollen derartige Tests schon in Kürze zur Verfügung stehen. Sie müssen aber für jede Rasse gesondert entwickelt werden, was mit einigem finanziellen Aufwand verbunden ist. Molekulargenetische Analysen werden aber zunehmend auch in der Humanmedizin von Bedeutung, weniger, um unsere „Abstammung“ zu verifizieren, als vielmehr um das Risiko, an einer bestimmten Krankheit zu erkranken und individuelle Medikamentenempfindlichkeit festzustellen. Und da sich die Pharmazie für uns westliche Zivilisationsmenschen darin ein gewaltiges Gewinnpotential sieht, wird der Fortschritt in der Bedeutung der oben erwähnten SNP nicht lange auf sich warten lassen.
Zurück zum Röntgenbild der Hüftgelenke. Auf einer korrekt erstellten Aufnahme ist auch der Übergang der Lendenwirbelsäule zum Kreuzbein ersichtlich. An diesem Übergang treten bei 0-20% der Hunde Missbildungen in Sinne eines Schaltwirbels oder Übergangswirbels auf. Es hat sich gezeigt, dass derartige Schaltwirbel das Risiko einer späteren Schädigung der Nerven im Rückenmark deutlich erhöhen. Auch eine ungleiche Entwicklung der Hüftgelenke wird damit in Zusammenhang gebracht. Es lohnt sich also, dieses Gebiet in Zukunft auch zu bewerten und im Befundblatt festzuhalten. Details dazu werden in einem weiteren Artikel folgen.
Der stärkste Ansporn zur Verbesserung der HD-Situation bei den Rassehunden wird ohne Zweifel vom kritischen und fordernden Käufer kommen. Er akzeptiert immer weniger, dass in gewissen weitverbreiteten Rassen jeder sechste Hund von fortgeschrittener HD betroffen ist. Bei dysplastischen Tieren verlangt er eine Kaufpreisminderung und die Übernahme der Behandlungskosten oder fordert gar den vollen Kaufpreis vom Züchter oder Verkäufer zurück. Ein Züchter fährt günstiger, wenn er eine wirksame Zuchtplanung einführt, als weiter nach eigenem Gutdünken Hunde zu paaren und die Augen vor den schlechten Resultaten zu verschliessen. Äusserst nachteilig für die Gesundheit einer Rasse ist es, die Röntgenbilder dysplastischer Hunde nicht offiziell beurteilen, sondern einfach verschwinden zu lassen. Damit betrügt der Besitzer nicht nur den Züchter um die jahrelangen Bemühungen um eine Verbesserung, sein Verhalten führt dazu, dass die HD-Statistiken völlig falsch ausfallen und damit weitgehend wertlos werden. Entsprechend wirkungslos sind dann natürlich auch die daraus abgeleiteten Vorschläge der Zuchtkommissionen. Noch übler schädigen jene Züchter ihre Rasse, die einen nicht gekörten Rüden zur Zucht verwenden und einen anderen als Vatertier angeben. Damit machen sie sich klar strafbar. Zudem wird die jahrelange Aufbauarbeit der anderen Züchter geschädigt. Der Schäferhunde-Klub ist solchen schwarzen Schafen auf die Schliche gekommen und verlangt deshalb einen Abstammungsnachweis mittels Blutuntersuchung (DNA-Analyse) der Zuchthunde.
Schliesslich kann der Gesetzgeber durch ein wirksames Tierschutzgesetz segensreiche Änderungen des Zuchtverhaltens auslösen. Im weiteren sind die Rasseklubs dazu aufgerufen, die unsinnige Ehrung eines einzelnen Champion of Champions abzuschaffen und dafür diejenigen Züchter zu belohnen, gesunde und langlebige Hunde züchten, die einem vernünftigen Rassestandard entsprechen. Nicht ein einsamer Spitzenhund garantiert eine gesunde Rasse, sondern eine breite Basis von gesunden und ausgewogen entwickelten Tieren.
Dr. M. Flückiger
Quelle: https://grsk.org/fuer_besitzer/was_ist_hd
Entstehung der ED
Der IPA, der FPC und die OCD treten bei Hunden im Alter von vier bis fünf Monaten während des stärksten Wachstumsschubes auf. Männliche Hunde sind häufiger betroffen, da sie in der Regel schneller wachsen als weibliche Tiere.
Die Erkrankungen werden dem Komplex der Osteochondrose zugerechnet. Als auslösender Mechanismus für die Entstehung der Osteochondrose wird eine Reifungsstörung des Knochens (Störung der enchondralen Ossifikation) verantwortlich gemacht, wobei sowohl der Knorpel der Wachstumsfugen (beim IPA) als auch der Gelenkknorpel (beim FPC und der OCD) betroffen sein kann. Die gelenkbildenden Knochen wachsen ungleichmäßig und es kann zur Überlastung besonders exponierter Bereiche im Gelenk kommen, mit der Folge einer Schädigung oder Ablösung von Knorpel- oder Knochenteilen.
Für den Processus anconaeus existiert bei großwüchsigen Hunden ein eigener Verknöcherungskern, der sich zwischen der 10. bis 14. Lebenswoche entwickelt. Die Fusion mit der Ulna erfolgt in Abhängigkeit von der Rasse zwischen der 13. und 20. Lebenswoche. Bei kleinen Hunden verläuft die Verknöcherung dagegen in der Regel von der Basis zur Spitze des Processus anconaeus. Liegt eine Störung der Verknöcherung dieser Wachstumsfuge vor, kann der Verknöcherungskern des Processus anconaeus nicht mit der Ulna verwachsen und die Fuge kann durch andauernde Belastung zerstört werden. So kommt es zur Loslösung des Processus anconaeus mit daraus resultierenden freien Gelenkkörper (Corpus librum) und Arthrosebildung.
Für den Processus coronoideus medialis der Ulna hingegen wurde bisher noch kein eigener Verknöcherungskern nachgewiesen, sondern es wird angenommen, daß die Verknöcherung von der Basis zur Spitze hin stattfindet, die mit der 20. bis 22. Woche abschließt. In dieser Zeit ist der mediale Kronenfortsatz besonders empfindlich gegenüber einer Überbelastung. Zur Überlastung kann es auch in Folge einer Stufenbildung im Gelenk kommen, nämlich dann, wenn die Ulna etwas länger ist als der Radius. Dadurch sind die Gelenkflächen dieser beiden Knochen nicht mehr auf einem Niveau und auf dem Processus coronoideus medialis der Ulna lastet vermehrt Gewicht, so dass er abbrechen kann. Gleiches kann auch passieren, wenn die Aussparung der Ulna, die die Oberarmgelenkwalze aufnimmt zu klein oder zu eng ausgebildet ist. Dadurch wird die Gelenkwalze nach vorne verlagert und es kann ebenfalls zu einer Überbelastung im Bereich des Processus coronoideus medialis der Ulna, aber auch des Processus anconaeus kommen.
Bei der OCD liegt eine lokale Spaltbildung bzw. Abtrennung des Gelenkknorpels vom darunterliegenden Knochen infolge einer gestörten Zelldifferenzierung im Gelenkknorpel vor. Betroffen ist immer der mediale (innere) Abschnitt der Oberarmgelenkwalze. Durch mechanische Beanspruchung entstehen Risse am Übergang zum gesunden Knorpel und es kann zur teilweisen oder vollständigen Ablösung der Knorpelschuppe kommen. Als Folge einer vollständigen Ablösung entsteht ein freier Gelenkkörper.
Fragmentierter Processus coronoideus medialis der Ulna (FPC) und Osteochondrosis dissecans der Trochlea humeri (OCD)
Vorkommen
Der FPC ist eine häufige Erkrankung des Ellbogengelenks mittelgroßer und großwüchsiger Hunderassen, aber auch kleinwüchsige Hunde können erkranken. Besonders oft sind Rottweiler, Retriever, Berner Sennenhunde, Deutsche Schäferhunde und Neufundländer betroffen. Aber auch andere mittelgroße und große Rassen und Mischlinge können erkranken. Gleichzeitig mit einem FPC kann eine OCD in einem Gelenk vorliegen, wobei hierfür Labrador und Golden Retriever, Berner Sennenhunde, Deutsche Schäferhunde und Neufundländer disponiert sind. Das alleinige Vorliegen einer OCD im Ellbogengelenk wird seltener beobachtet. Betroffen sind hier besonders Golden und Labrador Retriever. In der Mehrzahl der Fälle sind sowohl beim FPC als auch bei der OCD beide Ellbogengelenke betroffen.
Symptome und Diagnostik
Der Erkrankungsbeginn liegt für den FPC und die OCD im vierten bis fünften Lebensmonat. Erste Lahmheitssymptome können mit etwa vier bis sieben Monaten beobachtet werden. Am häufigsten beginnt die Lahmheit jedoch zwischen dem siebten und zwölften Lebensmonat. In manchen Fällen können die Symptome jedoch auch erst später auftreten. Bei alleiniger oder zusätzlicher OCD beginnt die Lahmheit meist etwas früher und tritt deutlicher in Erscheinung. Der FPC und die OCD verursachen ähnliche Beschwerden.
Es tritt eine ein- oder beidseitige gemischte Lahmheit unterschiedlicher Schwere auf, die oft nach Ruhe oder Belastung deutlicher sichtbar ist. In manchen Fällen ist nur eine Steifheit nach dem Liegen vorhanden oder die Lahmheit ist intermittierend (immer wiederkehrend). Insbesondere bei beidseitiger Erkrankung ist für den Besitzer das Erkennen von Beschwerden schwierig. Im Stand wird zur Entlastung des innen liegenden Gelenkabschnittes das Ellbogengelenk an den Körper herangezogen und die Vorderpfote nach außen gedreht. In der Vorführphase wird der Unterarm in Auswärtsstellung vorgeführt. Im weiteren Verlauf der Erkrankung als Folge der Lahmheit bildet sich die Muskulatur des Oberarms zurück (Muskelatrophie). Häufig ist eine vermehrte Gelenksfüllung vorhanden, und die passive Beugung und Streckung des Gelenks sowie Druck auf den inneren Gelenkabschnitt ist schmerzhaft. Bei längerer Erkrankungsdauer entwickeln sich sekundäre Arthrosen, wodurch das Gelenk verdickt und die Beweglichkeit eingeschränkt ist. Bei Bewegung des Gelenks können Reibegeräusche hörbar sein.
Röntgen
Zur Eingrenzung der klinischen Verdachtsdiagnose muß eine Röntgenuntersuchung des betroffenen Ellbogengelenks durchgeführt werden, wobei grundsätzlich beide Ellbogengelenke vergleichend in mindestens zwei Ebenen geröntgt werden sollten. Die Röntgendiagnostik des FPC ist jedoch oft sehr schwierig, da der Processus coronoideus medialis der Ulna von anderen Knochenstrukturen überlagert wird (Abb.4).
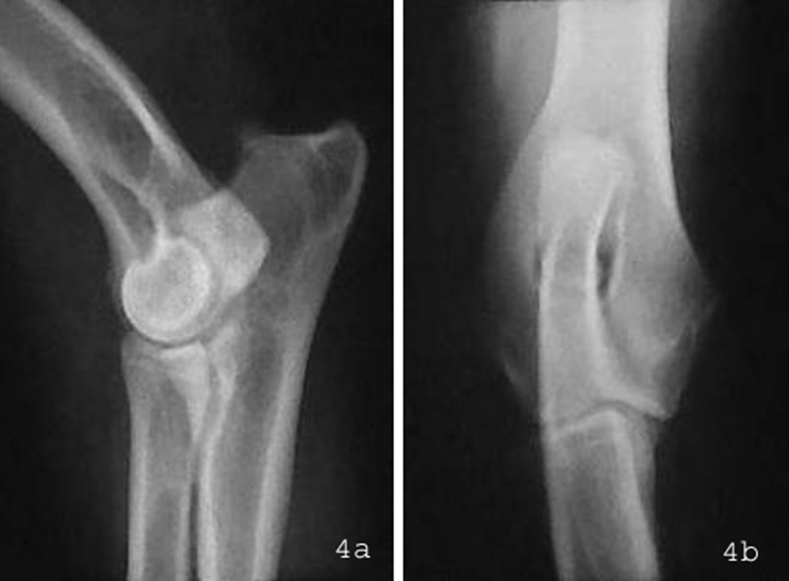
Abbildung 4: Röntgenaufnahmen von einem gesunden rechten Ellbogengelenk in (a) seitlichem (medio-lateral) Strahlengang und (b) von vorne (kranio-kaudal). Der Bereich des Processus coronoideus medialis der Ulna (Kreis) ist von anderen Knochenstrukturen überlagert
Die direkte Diagnose ist nur dann zu stellen, wenn der FPC deutlich verlagert ist. Ansonsten basiert die Verdachtsdiagnose eines FPC auf dem Vorliegen von anderen röntgenologischen Veränderungen, wie beispielsweise Stufenbildung, sekundäre Verdichtungen in der Knochenstruktur oder den im weiteren Verlauf der Erkrankung entstehenden Arthrosen. Diese sind etwa ab einem Alter von sieben bis neun Monaten röntgenologisch zunächst nur dezent zu erkennen und treten ab dem 12. Lebensmonat an verschiedenen Lokalisationen im Gelenk meistens deutlicher in Erscheinung (Abb.5).
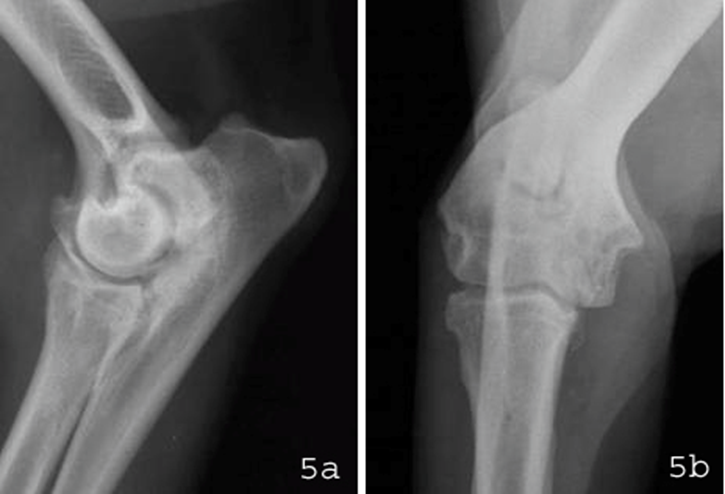
Abbildung 5: Röntgenbilder vom rechten Ellbogengelenk eines 4-jährigen Deutsch Drahthaar-Rüden mit FPC. Auf den Röntgenaufnahmen in seitlichem Strahlengang (a) und von vorne (b) sind deutliche Arthrosen an verschiedenen Lokalisationen erkennbar.
Allerdings sind die Arthrosen nicht für einen FPC oder eine OCD spezifisch, so dass die Verdachtsdiagnose durch weitere Untersuchungsverfahren, wie das Anfertigen von Schichtaufnahmen mit Hilfe der Computertomographie, der als Schlüssellochtechnik bekannten Arthroskopie (Abb.7) oder einer operative Darstellung bestätigt werden muß.

Abbildung 7: Jeweils ein rechtes Ellbogengelenk in arthroskopischer Darstellung von der Innenseite her. In der Mitte ist zur Orientierung als Skizze der einzusehende Gelenkabschnitt (Kreis) abgebildet: (a) gesundes Ellbogengelenk mit intaktem Gelenkknorpel über dem (1) Processus coronoideus medialis der Ulna, (2) der inneren und (3) der äußeren Gelenkwalze des Oberarms und (4) der angrenzenden Gelenkfläche des Radius. (b) Ellbogengelenk eines 4-monatigen Berner Sennenhundes mit einem FPC (*): im Bereich der Gelenkfläche des Processus coronoideus der Ulna (1) ist ein deutlich abgehobenes, mit Knorpel überzogenes Knochenstück zu erkennen. Der Gelenkknorpel der gegenüberliegenden inneren Gelenkwalze (2) ist noch intakt.
Prof. Dr. Andrea Meyer-Lindenberg
Quelle: https://grsk.org/fuer_besitzer/was_ist_ed
GRSK- Gesellschaft für Röntgendiagnostik
